UD 2. GLÚCIDOS.
UD 2. GLÚCIDOS.
MÍNIMOS EBAU, COORDINACIÓN DE BACHILLERATO 2023-2024
A.3. Biomoléculas orgánicas.
Biomoléculas orgánicas: Tipos, estructuras, propiedades y funciones. Grupos funcionales.
A.3.1. Características químicas, isomerías, enlaces y funciones de los monosacáridos (triosas, pentosas, hexosas en sus formas lineales y cíclicas), disacáridos y polisacáridos de mayor relevancia biológica.
A.3.1.1.- Glúcidos. Concepto.
A.3.1.1.1.- Monosacáridos:
-
Reconocimiento de fórmulas lineales y cíclicas (sin identificar los nombres de los monosacáridos).
-
Concepto de carbono asimétrico y de isomerías:
-
Estereoisómeros: D y L.
-
Anómeros: a y b.
-
A.3.1.1.1.1.- Triosas: gliceraldehído y dihidroxiacetona.
A.3.1.1.1.2.- Pentosas: ribosa, desoxirribosa y ribulosa.
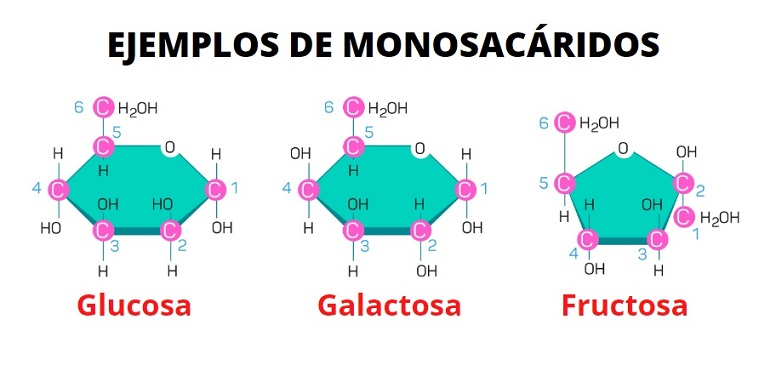
A.3.1.1.1.3.- Hexosas: glucosa, galactosa y fructosa.
A.3.1.1.2.- Disacáridos. Enlace O-glucosídico. Tipos: a y b.
A.3.1.1.2.1.- Disacáridos de interés biológico: maltosa lactosa, sacarosa y celobiosa (composición de cada uno y tipo de enlace (a o b), pero sin incluir fórmulas).
A.3.1.1.3.- Polisacáridos. Estructura, función y localización en los seres vivos.
A.3.1.1.3.1.- De reserva: almidón y glucógeno.
A.3.1.1.3.2.- Estructural: celulosa.
INTRODUCCIÓN GLÚCIDOS CONCEPTO
Los glúcidos son las biomoléculas orgánicas más abundantes de los vegetales. Éstos tienen sus estructuras esqueléticas de celulosa, sus reservas energéticas de almidón y sus líquidos internos, la savia elaborada con una alta concentración de sacarosa. En el mundo animal predominan las proteínas y los lípidos, con una excepción, los artrópodos, cuyo esqueleto externo es de quitina (también en hongos), un glúcido muy difícil de destruir.
Su función puede ser
- energética (fuente de energía para las células, como los monosacáridos),
- de reserva energética (acumulan monosacáridos y por tanto energía; son los disacáridos, el almidón y el glucógeno) o
- estructural (celulosa en la pared celular vegetal y quitina, en la pared celular de hongos y en el exoesqueleto de artrópodos)
1. GLÚCIDOS.
1.1. CONCEPTO DE GLÚCIDO
GLÚCIDO, del griego glykys, que significa “dulce”, aunque no todos los son.Los glúcidos son biomoléculas formadas básicamente por carbono (C), hidrógeno (H) y oxígeno (O), en una proporción semejante a CnH2nOn. Se les suele llamar hidratos de carbonos o carbohidratos. Este nombre es en realidad poco apropiado, ya que no se trata de átomos de carbono hidratados, es decir, unidos a moléculas de agua, sino de átomos de carbonos unidos a grupos alcohólicos o hidroxilos (-OH) y a radicales hidrógeno (-H).
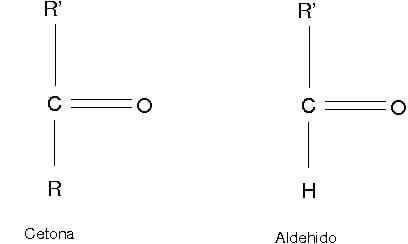
En todos los glúcidos siempre hay un grupo carbonilo, es decir un carbono unido a un oxígeno mediante un doble enlace. Este grupo carbonilo puede ser un grupo aldehído (-CHO) o bien un grupo cetónico (-CO-). Así pues, los glúcidos pueden definirse como polihidroxialdehídos o polihidroxicetonas.
Los glúcidos pueden sufrir procesos de aminación o de incorporación de grupos aminos (-NH2).
1.2. CLASIFICACIÓN DE LOS GLÚCIDOS
Según el esquema anterior los glúcidos se clasifican en:
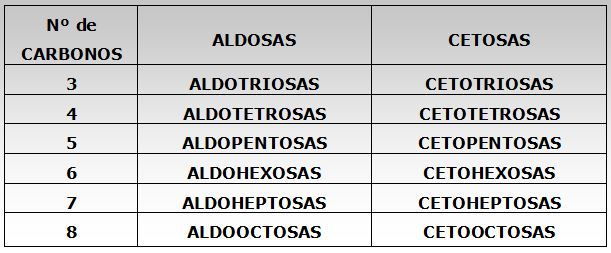
A. OSAS O MONOSACÁRIDOS: son los más simples; sus moléculas, sencillas y no hidrolizables, pueden tener entre 3y 9 átomos de C y constituyen las unidades, o monómeros, a partir de los cuales se originan los demás hidratos de carbono.-
A.1 ALDOSAS: el grupo carbonilo es aldehído, como la glucosa, ribosa o gliceraldehído.
-
A.2 CETOSAS: el grupo carbonilo es cetona, como la fructosa, ribulosa o dihidroxiacetona.
-
B.1 HOLÓSIDOS: en su composición intervienen exclusivamente sustancias glucídicas.
B.1.2. POLISACÁRIDOS: contienen más de 10 monosacáridos. A su vez distinguimos:
HOMOPOLISACÁRIDOS: constituidos por la repetición de un único tipo de monosacárido. Algunos ejemplos son el almidón, el glucógeno o la celulosa, compuestos exclusivamente de glucosa.
HETEROPOLISACÁRIDOS: en su composición intervienen dos o más clases de monosacáridos distintos. Algunos ejemplos son la hemicelulosa, la pectina o las gomas y mucílagos.
-
HETERÓSIDOS: en su composición participan sustancias glucídicas (monosacáridos) y otras no glucídicas de naturaleza variada. Dos ejemplos son los glucolípidos como los cerebrósidos y gangliósidos y las glucoproteínas como los peptidoglucanos (de la pared celular bacterina) y las inmunoglobulinas.
2. MONOSACÁRIDOS.
2.1. CARACTERÍSTICAS GENERALES - CONSIDERACIONES PREVIAS.
CONCEPTO. (ya visto) Los monosacáridos son glúcidos constituidos por una sola cadena polihidroxialdehídica o polihidroxicetónica. No pueden descomponerse mediante hidrólisis en otros glúcidos más sencillos. Constituyen los monómeros o unidades a partir de los cuales se forman el resto de los glúcidos. Por partes:
- Poseen de 3 a 7 átomos de carbono unidos entre si.
- A partir de 5 átomos de carbono pueden ciclar en disolución (formar estructuras cerradas). Estas pueden ser de 5C (pentosa o furanosa) o de 6C (hexosa o piranosa).
- Todos los átomos de carbono están unidos a un grupo funcional hidroxilo (-OH alcohol) o un grupo químicamente funcional llamado grupo carbonilo, es decir, un carbono unido a un oxígeno mediante un doble enlace. Este grupo carbonilo puede ser:
Un grupo cetónico (-CO). Un grupo aldehído (-CHO).
Por tanto, según el grupo carbonilo, los glúcidos pueden definirse como polihidroxialdehídos o polihidroxicetonas. Son polialcoholes con un grupo aldehído o cetona.
FUNCIONES: son muy variadas; energéticos (glucosa) y estructurales (ribosa y desoxirribosa - ARN y ADN). Los más importantes son la Glucosa, la Fructosa y la Ribosa.
PROPIEDADES:
- Propiedades físicas. Son sólidos cristalinos (sólidos), de color blanco o incoloros, hidrosolubles y de sabor dulce. Su solubilidad en agua se debe a los radicales hidroxilos (-OH) presentan una elevada polaridad. Presentan isomería espacial y óptica (ver más adelante)
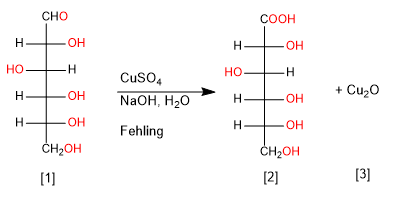
- Propiedades químicas. Los glúcidos son capaces de oxidarse (debido a la presencia de un grupo carbonilo que se oxida a un grupo carboxilo), es decir, de perder electrones, frente a otras sustancias que al aceptarlos se reducen = AZÚCAR REDUCTOR. Gracias a ello los glúcidos son la fuente básica de energía para las células.
2.2. TRIOSAS.
CONCEPTO y TIPOS.
Son glúcidos más sencillos, formados por 3 átomos de carbono. Hay dos triosas: una tiene un grupo aldehído y otra tiene un grupo cetónico. La aldotriosa se denomina gliceraldehído y la cetotriosa, dihidroxiacetona (fig.1). La fórmula molecular de ambas es C3H6O3. Son abundantes en el interior de la célula, ya que son metabolitos intermediarios de la degradación de la glucosa (glucolisis).
- Gliceraldehido presenta isomerías espaciales o esteroisómeros: D(+) gliceraldehído y L (-) gliceraldehído.
- La dihidroxiacetona no tiene ningún carbono asimétrico (único monosacárido) y, por lo tanto, isomerías ópticas.
ISOMERÍAS.
- Propiedad que consiste en la existencia de moléculas con la misma fórmula plana (química), pero con distinta estructura espacial y, por tanto, con distintas propiedades.
- Ello sucede siempre si hay una carbono asimétrico o quiral, es decir, cuando está unido a cuatro radicales diferentes. Se representa con un * y esta en todos los momosacáridos (excepto la dihidroxiacetona).
- Para representarlos se una la proyección de Fischer.
- El D-gliceraldehído, cuando el –OH está a la derecha y
- El L-gliceraldehído, cuando el –OH está a la izquierda del C2 - asimétrico
- Las estructuras enantiomorfas o ENANTIÓMEROS, formas D y L, difieren entre sí en la posición de todos los radicales – OH de los carbonos asimétricos; corresponden, pues, a la misma sustancia con las mismas propiedades físicas y químicas (densidad, punto de fusión, …), excepto la actividad óptica
- Se llamarán EPÍMEROS a los estereoisómeros en los que solo varía la posición del grupo -OH de uno de los carbonos asimétricos.
- Si la desviación es hacia la derecha, se denominan dextrógiras y se simbolizan con el signo (+). Así, por ejemplo, como el D-gliceraldehído es dextrógiro, se denomina D-(+) gliceraldehído.
- Sin embargo, si se desvía el plano de luz polarizada hacia la izquierda, se denominan levógiras y se simbolizan con el signo (-).
|
TIPO DE ISÓMERO |
DEFINICIÓN |
|
1. Isómeros espaciales o esteroisómeros |
Compuestos que tienen la misma forma molecular (misma composición química), pero diferente fórmula estructural o estructura espacial, debido a la diferente disposición de sus átomos. Pe: D y L-gliceraldehido. Un tipo de isomería es: |
|
1.1 Enantiómeros |
Isómeros en los que varía la posición de todos los –OH de los C asimétricos. Se trata de imágenes especulares no superponibles uno del otro. Los enantiómeros conservan el mismo nombre, añadiendo la indicación D o L. Se aplica la forma D cuando el - OH del último carbono asimétrico, y más alejado del grupo carbonilo, está a la derecha y la forma L cuando queda a la izquierda. Ejemplo: la D y L- glucosa |
|
1.2 Epímeros (se verá) |
Esteroisómeros en los que sólo varía la posición del grupo –OH de uno de los C asimétricos. Ejemplo: la D- glucosa y la D-galactosa, son epímeros en el C4 |
|
1.3. Isómeros ópticos |
Isómeros en el que uno de ellos desvía el plano de polarización de la luz polarizada hacia la derecha, y se designa (+), o dextrógiro, mientas que el otro la desvía en igual magnitud pero hacia la izquierda, y se designa (-) o levógiro. |
Ver vídeo RESUMEN AQUÍ
2.3. TETROSAS. no estudiar.
2.4. PENTOSAS.
-
En las aldopentosas, como hay tres carbonos asimétricos (C2, C3, C4), aparecen ocho posibles estructuras moleculares (23=8). En la naturaleza sólo se encuentran cuatro. La D-ribosa, en el ácido ribonucleico; la D-desoxirribosa, en el ácido desoxirribonucleico; la D-xilosa, que forma el polisacárido xilana de la madera; y la L-arabinosa, formando el polisacárido arabana, que es uno de los componentes de la goma arábiga (espesante natural - dar elasticidad a los caramelos)
-
Entre las cetopentosas aparecen cuatro estructuras moleculares (22=4) y cabe citar la D-ribulosa, que desempeña un importante papel en la fotosíntesis, debido a que se une a la molécula de dióxido de carbono (CO2), que queda así incorporada al ciclo de la materia viva.
2.5. HEXOSAS.
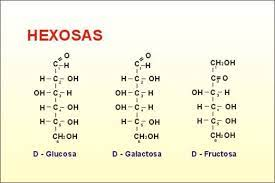
Son glúcidos con 6 átomos de carbono. Las aldohexosas tienen 4 C asimétricos y, por tanto, hay dieciséis posibles estructuras moleculares diferentes (24=16). Entre ellas tienen interés en biología la D(+) glucosa, la D(+) manosa y la D(+) galactosa. Entre las cetohexosas cabe citar la D(-) fructosa. Todas ellas en forma D.
Dado que la estructura abierta de las hexosas no es lineal, sino quebrada, debido a los ángulos que hay entre los enlaces de los C, los primeros y últimos C quedan relativamente próximos. Por ello, en disolución, la estructura lineal generalmente se cierra sobre sí misma formando un hexágono, parecido al de una molécula llamada pirano, o un pentágono, semejante al de una molécula llamada furano.
GLUCOSA:
-
Es el glúcido más abundante y la principal fuente de energía para la célula - respiración (las neuronas y los glóbulos rojos solo utilizan glucosa como fuente de energía). Es el llamado azúcar de uva.
-
Polimerizada da lugar a polisacáridos con función de reserva energética, como el almidón en vegetales o el glucógeno en animales (en hígado y músculo estriado), o con
-
Función estructural como la celulosa de las paredes vegetales.
-
En la naturaleza se encuentra la D (+) glucosa, también llamada por ello dextrosa ya que es muy dextrógira y la podemos encontrar en estado libre en frutos maduros como la uva, la miel, en el citoplasma celular y en el medio interno de los animales (en la sangre, glucemia)
GALACTOSA: No suele encontrarse libre en la naturaleza (salvo en orina de animales). Junto con la D-glucosa forma el disacárido lactosa, glúcido propio de la leche. También es un constituyente de determinados polisacáridos complejos (heteropolisacáridos) como las gomas, mucílagos y pectinas. Y en glucolípidos y glucoproteínas (glicocálix).
MANOSA: (no estudiar) es también una aldohexosa. Se encuentra en forma de D-manosa en ciertos tejidos vegetales. Aparece también como constituyente de ciertos polisacáridos (manosanas) presentes en bacterias, algas, hongos y algunos vegetales como el árbol del maná (Fraxinus ornus), cuyo exudado constituye el maná.
FRUCTOSA: es una cetohexosa. Se halla en forma β-D-fructofuranosa. Es fuertemente levógira, por lo que también se la denomina levulosa. Se encuentra libre en la fruta y, asociada con la glucosa, forma la sacarosa. En el hígado se transforma en glucosa. También aparece en el líquido seminal, donde actúa como nutriente de los espermatozoides.
CICLACIÓN de la GLUCOSA.
La glucosa al disolverse en agua, se hidrata, ya que el grupo carbonilo capta una molécula de agua. El hidrato así formado es inestable. El grupo carbonilo (-CHO) hidratado y situado en el C1 queda próximo al C5, y entre ellos reaccionan sus radicales -OH liberándose una molécula de agua y quedando ambos (C1 y C5) unidos por un átomo de oxígeno intramolecular. La molécula adquiere así forma de ciclo hexagonal, como la del pirano, por lo que se denomina glucopiranosa. El enlace que se ha formado entre el C1 y C5 se denomina hemiacetal (que es cómo se denomina la unión de un aldehído con un grupo alcohol (OH)). El grupo –OH que ahora pasa a tener el C1 se denomina hidróxilo hemiacetálico. Este C1 ahora es asimétrico y se denomina carbono anomérico. El estudio de la ciclación, resultado de la interacción entre grupos funcionales situados en C distantes, fue realizado por W.N. Haworth y se conoce con el nombre de proyección de Haworth.
CICLACIÓN MEDIANTE LA PROYECCIÓN DE FISCHER.
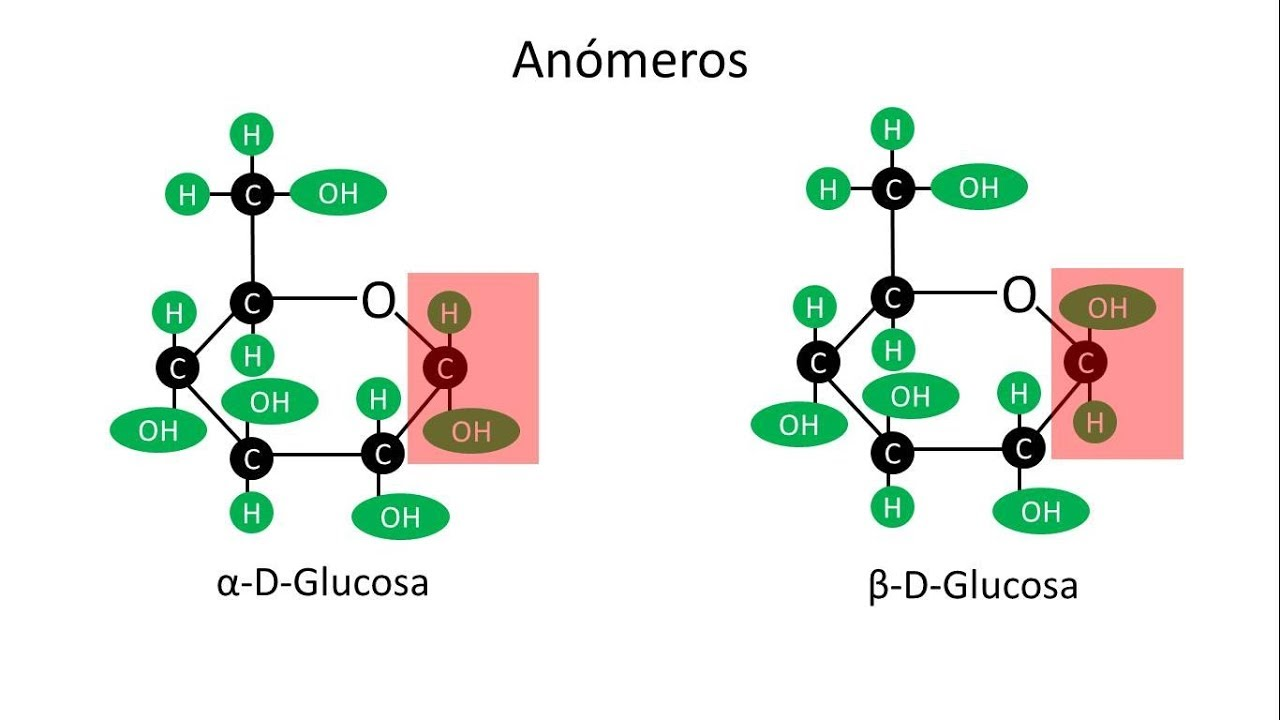
Según la posición del grupo –OH del C1 a un lado u otro del plano, se distinguen dos nuevas estructuras denominadas anómeros: el anómero α y el anómero β. El anómero es α cuando el grupo alcohólico (-OH) del C1 está en posición trans, es decir, al otro lado del plano donde está situado el C6H2OH portado por el C5. El anómero es β cuando los dos radicales están en posición cis, es decir, en el mismo lado del plano.
¿alfa o beta? según posición del grupo -OH del C1. ¿Recuerda formas D o L? ¿y + o -?
En realidad, las estructuras cíclicas de la glucosa no son planas, como indican los modelos estudiados, sino que pueden adoptar dos conformaciones en el espacio: la conformación nave o bote y la conformación silla (más estable). Ello se debe a que los enlaces se orientan en el espacio y no en el plano.
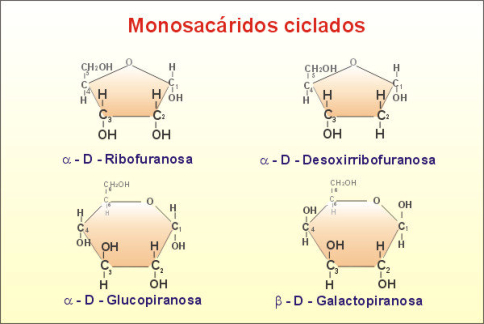
La ciclación puede adoptar también la estructura pentagonal del furano, como sucede, por ejemplo, en la ribosa y en la dexosirribosa, que se denominan por ello ribofuranosa y desoxirribofuranosa. Como sólo son posibles los anillos de cinco o más átomos de carbono, las triosas y las tetrosas siempre tienen estructuras abiertas. El resto de monosacáridos, cuando se disuelven, presentan un equilibrio entre la forma cíclica y la forma abierta. En el caso de la glucosa, la estructura lineal nunca llega al 5% del total.
3. DISACÁRIDOS.
3.1 EL ENLACE O-GLUCOSÍDICO
El enlace O-glucosídico es un tipo de enlace que se establece entre dos monosacáridos. Este enlace se establece entre dos grupos –OH de dos monosacáridos que quedan enlazados por un átomo de oxígeno. La formación de un disacárido se denomina síntesis por condensación o deshidratación debido a la liberación de una molécula de agua. El enlace O-glucosídico puede ser α-glucosídico si el primer monosacárido es α, y β-glucosídico si el primer monosacárido es β. Por ejemplo, entre el C1 de una α-D-glucopiranosa y el C4 de otra D-glucopiranosa (α o β) se establece un enlace tipo α (14). Este enlace puede ser de dos tipos: VER ANIMACIÓN ¿alfa o beta? según posición del grupo -OH del C1.
Enlace monocarbonílico, el enlace se establece entre el grupo –OH del carbono anomérico del primer monosacárido y el –OH de un carbono no anomérico del segundo monosacárido, es decir, solo interviene el grupo –OH de un C cabonílico. Al quedar un carbono anomérico con el hidroxilo hemiacetálico libre, la molécula es reductora (tiene la capacidad de reducir el reactivo de Fehling). Por ejemplo la maltosa, la celobiosa y la lactosa. Para denominarlos se hace con el nombre del primer monosacárido terminado en –osil y la del segundo monosacárido terminado en –osa.
-
Enlace dicarbonílico, el enlace se establece entre los dos grupos -OH de los dos carbonos anoméricos de los dos monosacáridos, con lo que se pierde la capacidad de reducir el reactivo de Fehling, es decir, la molécula resultante será no reductora, como por ejemplo la sacarosa. Para denominarlos se hace con el nombre del primer monosacárido terminado en –osil y la del segundo monosacárido terminado en –ósido.
3.2 DISACÁRIDOS CON IMPORTANCIA BIOLÓGICA
Son sólidos cristalinos, blancos, dulces y solubles en agua. Los principales son:
-
MALTOSA (glucosa + glucosa α (14)): disacárido formado por dos moléculas de D-glucopiranosa unidas mediante enlace α (14). La maltosa se encuentra en el grano germinado de cebada y otras semillas. La cebada germinada artificialmente se utiliza para la fabricación de cerveza, y tostada se emplea como sustitutivo del café, es la llamada malta. Se obtiene por hidrólisis del almidón y glucógeno llevada a cabo por amilasa de la saliva, jugos pancreáticos e intestinales. La maltosa se degrada en dos glucosas por la maltasa.
-
CELOBIOSA (glucosa + glucosa β (14)): disacárido formado por dos moléculas de D-glucopiranosa unidas mediante enlace β (14). No se encuentra libre en la naturaleza. Se obtiene por hidrólisis de la celulosa. Es hidrolizada en dos glucosas por la celobiasa o β (14) glucosidasa que sólo está presenten en microorganismos (ej flora intestinal hervíboros), aunque también se ha detectado en termitas (xilófagos), caracoles y gusanos de tierra.
-
LACTOSA (galactosa + glucosa β (14)): disacárido formado por una molécula de D-galactopiranosa y otra de D-glucopiranosa unidas por un enlace β (14). Se encuentra libre en la leche de los mamíferos. Durante la digestión química se hidroliza por medio de la enzima lactasa. Durante la digestión se hidroliza por la enzima lactasa. Algunas personas después de la lactancia dejan de producir lactasa por tanto la lactosa se acumula en la luz del tubo digestivo y empieza a entrar agua por ósmosis lo que produce diarrea, vómitos y dolor. Es lo que se denomina intolerancia a la lactosa la cual se hereda en un gen autosómico recesivo.
-
SACAROSA (glucosa + fructosa α (12)): disacárido formado por una molécula α-D-glucopiranosa y otra de β-D-fructofuranosa unidas por medio de un enlace α (12). Se encuentra en la caña de azúcar y en la remolacha azucarera y es un componente principal de la savia elaborada. El enlace se realiza entre el –OH del C1 anomérico del primer monosacárido –glucosa- y el –OH del C2 anomérico del segundo monosacárido –fructosa-. Debido a ello es el único disacárido de los citados que no es reductor, es decir no es capaz de reducir el reactivo Fehling. Enzima que la degrada = sacarasa, en glucosa y fructosa.
- El segundo es una celobiosa que no podemos digerir. Lo identificamos por estar formado por dos glucosas unidas por enlace beta 1-4. glucosa + glucosa β (14)
- El último, el C, es una maltosa (glucosa + glucosa α (14)). La maltosa es el producto de la digestión del glucógeno y almidón (enzima = amilasa de la saliva, pancreática e intestinal) presente en cereales (pan, pastas, tortitas, arroz, legumbres...) y tubérculos. Los alimentos que contienen maltosa son la cebada germinada y la cerveza, por ello, no podemos llamarlo azúcar en este ejercicio, aunque su degradación contribuye notablemente al aumento de la glucosa en sangre (como digestión del almidón, componente principal de todas las dietas)
4. POLISACÁRIDOS (ÓSIDOS).
Los polisacáridos están formados por la unión de muchos monosacáridos (puede variar de once a varios miles) mediante enlace O-glucosídico, con la consiguiente pérdida de una molécula de agua por cada enlace.
Los polisacáridos tienen las siguientes propiedades:
-
Pesos moleculares muy elevados.
-
No tienen sabor dulce.
-
No son cristalinos.
-
Por su gran tamaño suelen ser insolubles como la celulosa o formar dispersiones coloidales como el almidón. Pero sus numerosos grupos OH les permite retener y absorber agua.
-
No son reductores (no pueden reducir el reactivo de Fehling), pues no contienen carbonos anoméricos con sus grupos hidroxilos libres (Ocupados en los enlaces O-glucosídicos) .
Pueden desempeñar funciones estructurales o de reserva energética.
-
Los polisacáridos que realizan una función estructural presentan enlace β-glucosídico (enlace muy resistente a la hidrólisis), y los que llevan a cabo
-
función de reserva energética presentan enlace α-glucosídico (se hidroliza fácilmente liberando monosacáridos – aporte energético rápido)
Los polisacáridos se clasifican en:
|
HOMOPOLISACÁRIDOS, de glucosa |
Mediante enlace α (función de reserva energética) |
ALMIDÓN |
|
GLUCÓGENO |
||
|
Mediante enlace β (función estructural) |
CELULOSA |
|
|
QUITINA |
||
|
HETEROPOLISACÁRIDOS |
Mediante enlace α |
PECTINA |
|
AGAR-AGAR |
||
|
GOMA ARÁBIGA |
4.1 EL ALMIDÓN
El almidón es el polisacárido de reserva energética propio de los vegetales. Se acumula en forma de gránulos dentro de la célula vegetal, en el interior de los plastos (amiloplastos). En el almidón se encuentran unidas cientos o miles de moléculas de glucosa formando una dispersión coloidal. Al no estar disueltas en el citoplasma, como ocurre con las moléculas de glucosa libres, no influye en la presión osmótica interna y constituyen una gran reserva energética que ocupa poco volumen.
Los depósitos de almidón se encuentran en las semillas de los cereales (trigo, maíz, arroz…), en los tubérculos, como la patata y el boniato, en las legumbres y en las raíces. A partir de ellos, las plantas pueden obtener energía sin necesidad de luz, imprescindible durante la noche y para la supervivencia de las semillas.
El almidón está integrado por dos tipos de polímeros: la amilosa que constituye el 30% del peso y la amilopectina que constituye el 70%.
-
AMILOSA. Está constituida por un polímero de maltosas unidas mediante enlaces α (14). Su estructura es helicoidal con seis moléculas de glucosa (tres maltosas) por vuelta. Su peso molecular varía desde varios cientos a 500.000 Da o uma. Es soluble en agua y forma dispersiones coloidales. Con el yodo se tiñe de color azul negruzco. Por hidrólisis por la acción de la enzima α-amilasa en los animales (saliva y jugo pancreático) o de la β-amilasa, propia de las semillas, da lugar primero a un polisacárido menor denominado dextrina y luego a maltosa. La maltosa, luego mediante la acción de la enzima maltasa, pasa a D-glucosa.
AMILOPECTINA. Está constituida por un polímero de maltosas unidas mediante enlaces α (14), con ramificaciones en posición α (16). Las ramas tienen alrededor de doce glucosas. No es, pues, una estructura lineal sino ramificada. Su peso molecular puede llegar a 1.000.000 Da, y es menos soluble en agua que la amilosa. Con el yodo se tiñe de rojo oscuro. Por hidrólisis con la α-amilasa o con la β-amilasa aparecen moléculas de maltosa y los núcleos de ramificación que, por poseer enlaces (16), son inatacables por estas enzimas (amilasas). Estos núcleos reciben el nombre de dextrina límite. Sobre ellos sólo actúa la enzima R-desramificante (amilopectina-1,6-glucosidasa), específica del enlace (16). Tras el concurso de la maltasa se obtiene finalmente la D-glucosa.
4.2 GLUCÓGENO
El glucógeno es el polisacárido de reserva energética propio de los animales. Se encuentra abundantemente en el hígado, donde constituye la reserva general del organismo y en los músculos, reserva exclusiva de los mismos. Forma dispersiones coloidales en el interior de la célula.
El glucógeno, al igual que la amilopectina, está constituido por un polímero de maltosas unidas mediante enlaces α (14), con ramificaciones en posición α (16), pero con mayor abundancia de ramas. Éstas aparecen aproximadamente, cada ocho o diez glucosas. Tiene hasta unas 15000 moléculas de maltosas. Su peso molecular oscila entre 1 y 5 millones de Da. Con el yodo, la dispersión coloidal se tiñe de rojo oscuro. Las enzimas amilasas sobre el glucógeno dan maltosas y dextrina límite. Luego, mediante las enzimas R-desramificantes y las maltasas, se obtiene D-glucosa.
4.3 CELULOSA
La celulosa es un polisacárido con función estructural propio de los vegetales. Es el primer polisacárido más abundante de la biosfera. Es el elemento principal de la pared celular. Esta pared constituye una especie de estuche en el que queda encerrada la célula vegetal, y que persiste tras la muerte de la célula. Las fibras vegetales (algodón, lino, cáñamo, esparto, etc.) y el interior del tronco de los árboles (el leño o la madera) están básicamente formados por paredes celulósicas de células muertas. El algodón es casi celulosa pura, mientras que la madera tiene un 50% de otras sustancias que aumentan su dureza, como la lignina y suberina.
La celulosa es un polímero de β-D-glucopiranosas unidas mediante enlaces β (14). Dos de ellas forman una celobiosa. Cada polímero tiene de 150 a 5000 moléculas de celobiosas, y un peso molecular medio de 800000 Da. Estos polímeros forman cadenas moleculares no ramificadas, que se pueden disponer paralelamente uniéndose mediante puentes de hidrógeno, en agregados cristalinos muy ordenados. El conjunto de cadenas (de 60 a 70) se denomina micelas y solo son visibles al ME de alta resolución. Las micelas se unen formando microfibrillas (comprende 20 micelas), que a su vez se agrupan dando macrofibrillas o fibrillas (comprende 250 microfibrillas), ya observables al microscopio óptico. Éstas se unen formando fibras de algodón (comprende 1500 fibrillas), que son observables a simple vista. Una fibra está constituida por unas 8 x 108 cadenas de celulosa.
La peculiaridad del enlace β (14) hace a la celulosa inatacable por las enzimas digestivas humanas; por ello, este polisacárido no tiene interés alimentario para el hombre. Los insectos xilófagos, como las termitas y los herbívoros rumiantes (vaca, oveja, cabra, camello), aprovechan la celulosa gracias a los microorganismos simbióticos del tracto digestivo, que producen celulasas. Los rumiantes, como la vaca, tienen un voluminoso estómago (poligástricos - 4 estómagos) que les sirve como tanque de fermentación para estos microorganismos; por ello en sus heces no hay restos celulósicos, sin embargo, en los herbívoros no rumiantes como el caballo, sí los hay.
4.4 QUITINA
La quitina es un polímero de N-acetil--D-glucosamina unido mediante enlaces β (14), de modo análogo a la celulosa. Como ella, forma cadenas paralelas, muy resistentes e insolubles en agua. Es el segundo polisacárido más abundante de la biosfera y participa como componente esencial en la construcción de la pared celular de bacterias y hongos y del exoesqueleto de los artrópodos.
4.5 OTROS POLISACÁRIDOS
Todos los polisacáridos estudiados hasta ahora pertenecen al grupo de homopolisacáridos (polímeros de un solo tipo de monosacárido), sin embargo, aunque los heterospolisacáridos son menos importantes vamos a estudiarlos muy someramente. Los heteropolisacáridos son sustancias que por hidrólisis dan lugar a varios tipos distintos de monosacáridos o derivados de éstos. Los principales son:
-
Pectina. Se encuentra en la pared celular de los tejidos vegetales. Abunda en la manzana, pera, ciruela y membrillo. Posee una gran capacidad gelificante que se aprovecha para preparar mermeladas.
-
Agar-Agar. Se extrae de las algas rojas o rodófitas. Es muy hidrófilo y se utiliza en microbiología para preparar medios de cultivo o en cocina como gelificante.
-
Goma arábiga. Es una sustancia segregada por las plantas para cerrar sus heridas = resina.
-
Ácido hialurónico y la condroitina. También denominados glucosaminoglucanos o mucopolisacaridos por el aspecto viscoso que tienen sus disoluciones, y suele asociarse a determinadas proteínas para formar las mucinas, también llamadas proteoglucanos.
-
Heparina. Su función consiste en impedir la coagulación de la sangre.
RESUMEN...
-
FUNCIONES DE LOS GLÚCIDOS
Las funciones más importantes son las siguientes:
-
Función estructural. Forma parte de diversas estructuras, ya sean moleculares, celulares u orgánicas. Por ejemplo, la ribosa y la desoxirribosa (en ácidos nucleicos), la celulosa, hemicelulosa y pectinas (en paredes celulares), y la quitina (en el exoesqueleto de los artrópodos). Esta función estructural la desempeña gracias a los enlaces β-glucosídicos lo que origina estructuras muy estables, ya que la mayoría de organismos carecen de enzimas para romper este enlace.
-
Función energética. Los azúcares constituyen una fuente primaria de energía química para las células. En una oxidación completa producen 410 Kcal/100g. El azúcar energético por excelencia es la glucosa ya que es el monosacárido más abundante en el medio interno y además puede atravesar la membrana plasmática sin necesidad de ser transformada en moléculas más pequeñas.
-
Función de reserva energética. Los glúcidos son convertidos a polisacáridos para el almacenamiento de energía. Es el caso de macromoléculas como el almidón en los vegetales y el glucógeno en los animales. En esta forma se pueden almacenar centenares de moléculas de glucosa sin que ello implique un aumento de la concentración del citoplasma lo que provocaría que entrase agua a la célula por ósmosis.
-
Marcadores de destino celular y lugares de reconocimiento celulares. Son transportadores de información biológica. Son sobre todos oligosacáridos unidos a proteínas y situados en la membrana plasmática, que exhiben un mensaje de reconocimiento celular a otras células.
-
Intermediarios metabólicos. Forma parte de moléculas intermedias en muchas reacciones de degradación y de síntesis, como por ejemplo el gliceraldehído o la dihidroxiacetona.
-
Funciones especiales. Como por ejemplo función antibiótica (estreptomicina), vitamínica (vitamina C), anticoagulante (heparina), hormonal (hormonas de la hipófisis), inmunitaria (inmunoglobulinas o anticuerpos), etc.
2. Diferencias entre almidón, glucógeno y celulosa.
|
|
ALMIDÓN |
CELULOSA |
GLUCÓGENO |
|
Naturaleza química |
Glúcido homopolisacárido de glucosa con enlace α
|
Glúcido homopolisacárido de glucosa con enlace β |
Glúcido homopolisacárido de glucosa con enlace α
|
|
Función |
Reserva energética en vegetales |
Función estructural en vegetales |
Reserva energética en animales |
|
Lugar de la célula donde se localiza |
Se acumula en forma de gránulos en el interior de los amiloplastos. Abunda en semillas y tubérculos como la patata. |
La celulosa es el elemento principal de la pared celular de las células vegetales. |
Se acumula en forma de gránulos en el interior de las células hepáticas y musculares. |
|
Diferencias estructurales |
Está formado por dos polímeros:
|
Formada por un polímero lineal de β-D glucosas unidas mediante enlace β (14). Las cadenas lineales se unen mediante puentes de hidrógenos intracatenarios. Las cadenas lineales se organizan en micelas (60 ó 70 cadenas lineales) Microfibrillas (20 micelas) Macrofibrillas o fibrillas (250 microfibrillas) Fibras de algodón (1500 fibrillas). |
La estructura del glucógeno es similar a la amilopectina del almidón pero con más ramificaciones.
Consta de un polímero de α-D glucosas unidas mediante enlace α (14) con ramificaciones en α (16) cada 8 ó 10 glucosas.
|
3. Localización y función de algunos glúcidos
|
|
LOCALIZACIÓN |
FUNCIÓN |
|
GLUCOSA |
Se encuentra libre en el citoplasma celular en frutos como la uva o los dátiles. Se almacena en forma de reserva (almidón o glucógeno) y forma parte de la celulosa de la pared. |
Es el principal nutriente de los seres vivos. Se oxida en la respiración celular. |
|
RIBOSA |
Se localiza en nucleótidos y ácidos nucleicos |
Componente estructural de los nucleótidos libres como el ATP y ácidos nucleicos como el ARN. |
|
DIHIDROXIACETONA |
Abundante en el citoplasma de la célula |
Metabolito intermediario de la degradación de la glucosa. |
|
FRUCTOSA |
Se encuentra libre en la fruta y asociado a la glucosa forma la sacarosa. |
Es el principal nutriente de los espermatozoides y en las células hepáticas se convierte en glucosa. |
|
GALACTOSA |
No se encuentra libre, se puede hallar en la orina de animales. |
Forma parte de la lactosa de la leche al unirse a la glucosa. |
|
RIBULOSA |
Se localiza en el interior celular. Abunda en los cloroplastos. |
Actúa como intermediario en la fijación del carbono (CO2) en la fotosíntesis. |
|
GLICERALDEHÍDO |
Abunda en el citoplasma de la célula. |
Metabolito intermediario de la degradación de la glucosa. |
A. Polisacáridos. (0,5 puntos)
C. ADN (aquí, además, nombra los elementos que componen el monómero). (0,75 puntos)No hacer.
8. EBAU 17 Indique dos diferencias y dos semejanzas entre almidón y celulosa (1punto)
9. A partir de la descripción dada identifica la biomolécula y, a continuación, explica sus funciones en la célula: (0,5 puntos cada apartado)
A) Polímero que recubre las células vegetales.
B) Polímero glucídico abundante en las células del hígado y células musculares.
C) Monómero integrante de los 2 polímeros anteriores.
D) Biomolécula anfipática (anfipolar) rica en ácido fosfórico y ácidos grasos. No hacer.
10. EBAU 18 Glúcidos. Cita un polisacárido de reserva indicando:
A) Estructura y composición. (1.5 puntos)
B) Función y localización. (0.5puntos)
11. En relación a los polisacáridos, proteínas y ácidos nucleicos identifica: (1 punto cada apartado) Sólo de polisacáridos.
A) Monómeros que permiten su síntesis
B) Enlaces químicos que los unen.
12. EBAU 2015 junio. Pared Celular Vegetal.
A. Estructura y composición química.
B. Funciones.
13. EBAU 2015 jul. Cite un polisacáridos de reserva animal indicando:
A Estructura y composición (1,5p)
B Función y Localización (0,5p)
- Mastica un poco de miga de pan y describe su sabor.
- ¿Qué molécula glucídica mayoritaria se encuentra en este alimento?
- Compáralo con el sabor de un terrón de azúcar.
- ¿Qué semejanzas y qué diferencias existen entre los componentes de ambos alimentos?
Interpreta el gráfico y elabora las conclusiones pertinentes
- muestra 1: rojo;
- muestra 2: incoloro;
- muestra 3: incoloro.
- muestra 2: incoloro,
- muestra 3: rojo.
PAU 2025. GLÚCIDOS - COMPETENCIALES.
1. PAU25 Extraord La Rioja 2025. Los monosacáridos pueden existir en la naturaleza en diferentes formas estructurales:
a) ¿Qué son los monosacáridos? (0,1 puntos)
b) Explique en qué formas podemos encontrarlos en la naturaleza (0,2 puntos).
c) ¿Qué son las estructuras D y L de los carbohidratos? ¿Qué relación tiene esto con los conceptos de
enantiómeros, epímeros o diastereoisómeros? (0,7 puntos)
Solución apartado c)
Las configuraciones D y L de los carbohidratos se refieren a la orientación del grupo hidroxilo (-OH) en el último carbono quiral, siendo D cuando está a la derecha y L cuando está a la izquierda en una proyección de Fischer.
- Estereoisómeros: son enantiómeros si son imágenes especulares no superponibles (D-glucosa vs L-glucosa)
- Diastereoisómeros si difieren en otros carbonos quirales pero no son imágenes especulares (por ejemplo, D-glucosa vs D-galactosa).
- Los epímeros son un tipo especial de diastereoisómeros que solo difieren en un carbono quiral.
2. PAU25 Extraord Andalucía 2025.
Pregunta 2.1 (2 puntos) En una situación experimental, tras permanecer en ayunas, tres personas ingieren: la primera (A) una ración de celulosa; la segunda (B) una ración de glucosa; y la tercera (C) una ración de almidón.
Ordene los tres casos en función de la rapidez con la que aumentará la glucemia (nivel de glucosa en sangre). Justifique su respuesta [0,6].
Cite tres propiedades de los polisacáridos [0,6] y
Explique la composición e importancia biológica de un polisacárido de origen vegetal [0,4].
Indique dos características exclusivas de las células vegetales y nombre la función que corresponde a cada característica [0,4].
3. PAU25 Ord Canarias 2025.2. En el folleto divulgativo se informa “La alergia a la leche (más concretamente, a sus componentes como la caseína, la β-lactoglobulina …) no es lo mismo que la intolerancia a la lactosa, debida a que las persona tienen una ausencia o bajo nivel de la lactasa”. (Fuente: Agencia Española de Seguridad Alimentaria y Nutrición, AESAN).
a. Indica las unidades estructurales de cada una de las biomoléculas del texto (negrita).
b. Indica el nombre del enlace de unión de las citadas unidades básicas.
c. Dibuja la estructura básica y común de las unidades que constituyen a la lactasa.
d. Indica cuál es la composición de un heterósido.
4. Mod 25 Ord Cantabria.2Pregunta 1 [1,25 PUNTOS] Dibuje las reacciones de formación de los enlaces O-glucosídico, éster, y peptídico, nombrando los grupos que participan y los productos que se forman. Mencione un ejemplo de biomolécula que contenga cada uno de dichos enlaces. Pregunta 2 [1,25 PUNTOS] Escriba un texto de no más de 10 líneas en el que se relacionen de manera coherente, dentro de un fenómeno biológico, los siguientes conceptos: enzima, centro activo, velocidad máxima, desnaturalización. Pregunta 1. Opción A. La intolerancia a la lactosa se debe a la deficiencia de un enzima disacaridasa, la lactasa, de modo que no es posible la ruptura de la lactosa, no puede ser absorbida y se acumula en el intestino delgado. Esta acumulación provoca que las células intestinales pierdan agua, y ello causa diarrea y deshidratación. a. Indica cómo se llama el enlace que rompe la lactasa y haz un esquema de cómo se forma dicho enlace. (Calificación 1p) b. Pon un ejemplo de glúcido con función de reserva de energía y otro con función estructural (Calificación 1 punto) c. ¿Por qué la acumulación de lactosa en el intestino provoca que las células intestinales pierdan agua? (Calificación 0.5 puntos)
5. PAU25 Extraord Canarias 2025.24. La creciente demanda de productos de consumo más saludables ha llevado a un interés renovado por entender y aprovechar los beneficios de los glúcidos dentro de la industria alimentaria (Fuente: The Food Tech, 2024).
a. Clasifica a los glúcidos en base a la complejidad de la biomolécula.
b. ¿Cuál es la importancia biológica de la celulosa?
c. Cita 2 funciones de los glúcidos en una célula animal.
d. Define el enlace o-glucosídico.
6. PAU25 Ord Canarias 2025.2La OMS considera una dieta equilibrada en nutrientes la que contiene aproximadamente la siguiente proporción en kcal: las proteínas no deben sobrepasar el 15%; los lípidos no deben sobrepasar el 30% y los glúcidos es el resto hasta el 100%.
a. La imagen adjunta corresponde a distintos componentes moleculares. Identifica y especifica aquellos que pueden ser componentes del grupo de biomoléculas resaltadas en negrita en el texto.
b. Los polímeros con glucosa son el almidón y el glucógeno, indicando la función de cada uno.
c. Indica cuál es la composición de un heteropolisacárido.
d. Indica qué molécula glucosídica es constituyente de cada tipo de ácido nucleico.
7. Modelo 25 País Vasco. Opción 2B A pesar de estar formadas por la misma molécula básica, la celulosa y el almidón tienen funciones y estructuras muy diferentes. a) (1,0 punto) - ¿De qué molécula sencilla están formadas estas dos macromoléculas? - ¿En qué formas anoméricas se presentan en la celulosa y en el almidón? - Nombra y describa los enlaces que unen a estos monómeros. b) (1,0 punto) Enumere las principales funciones de estas dos macromoléculas. c) (0,40 puntos) Exponga razonadamente la causa por la que podemos digerir el almidón y no la celulosa.
8. PAU25 Extraord Murcia 2025.Bloque 1: BIOMOLÉCULAS. BIOLOGÍA CELULAR. METABOLISMO. Conteste UNA de las dos preguntas siguientes (1,5 puntos):
1.1. Según se describe en la guía metabólica del Hospital Materno-infantil Sant Joan de Deu de Barcelona,
“la enfermedad de Pompe o glucogenosis tipo II es un trastorno metabólico causado por una acumulación
de glucógeno en múltiples tejidos, principalmente el músculo, provocando insuficiencia cardiaca, motora y
respiratoria progresivas. Es debida a la deficiencia de una enzima lisosomal que rompe enlaces oglucosídicos
denominada maltasa ácida”.
A) Indique qué tipo de biomolécula es el glucógeno y su función en las células (0,25 puntos).
B) Explique por qué la deficiencia de la enzima maltasa ácida provoca un acúmulo de glucógeno en la
célula (0,3 puntos).
C) Mencione otra biomolécula que desempeñe la misma función en la célula y describa su estructura
general (0,4 puntos).
D) Mencione una vía catabólica que forme parte, tanto del proceso de degradación del glucógeno, como
del proceso de degradación de la
9. PAU25 Extraord Cantabria 2025.APARTADO 1 [1,25 puntos]. Bloque A. Las biomoléculas. Conteste a las preguntas de UNA SOLA de las siguientes opciones. Opción 1 [1,25 puntos].
Para entretener a los bebés es habitual darles un trocito de pan seco para que lo mastiquen. Con el tiempo, la acción enzimática de la saliva lo vuelve dulce y les gusta. a) ¿Cómo se denomina la enzima responsable de este fenómeno y cuál es el enlace que rompe? b) ¿Sobre qué polímero está actuando y a qué familia de biomoléculas orgánicas pertenece dicho polímero? c) Indique otro polímero formado por las mismas subunidades, pero con una función estructural y no asimilable por los animales. d) Compare las estructuras de ambos polímeros y explique el motivo de las diferencias entre ellos.
10. PAU25 Extraord Navarra 2025.Las biomoléculas
2. TEBRIO es una empresa líder a nivel mundial que utiliza la quitina para aplicaciones bio-industriales,
como la fabricación de plásticos biodegradables. a) ¿A qué grupo de biomoléculas pertenece la quitina y en
qué seres vivos podemos encontrarla? (0.75 P) b) La quitina se mezcla con otros polímeros naturales como
la celulosa para mejorar flexibilidad y resistencia: ¿Qué diferencias estructurales tiene la quitina respecto a
la celulosa? (0.25 P)
11. PAU25 Extraord Madrid 2025.2. B.- En relación con las biomoléculas En dos envases de distintos tipos de galletas aparece la información nutricional que se muestra en las siguientes tablas:
a) Compare la información nutricional de los dos tipos de galletas y determine cuál de ellas tiene mayor valor energético y cuál mayor contenido en sal por cada 100 g (0,5 puntos).
b) Los hidratos de carbono presentes en la galleta son de varios tipos. Según la AESAN (Agencia Española de Seguridad Alimentaria y Nutrición), el término azúcares añadidos hace referencia a monosacáridos y disacáridos. Ponga cuatro ejemplos de estos tipos de hidratos de carbono (0,5 puntos).
c) El otro tipo de hidrato de carbono presente es la fibra alimentaria. Indique cuál es el componente principal de la fibra y señale qué efecto beneficioso tiene en el organismo (0,5 puntos).
d) Teniendo en cuenta las cantidades de los distintos tipos de grasas saturadas e insaturadas presentes, explique cuál de los dos tipos de galletas sería menos perjudicial para una persona que quiera disminuir el riesgo de padecer enfermedades cardiovasculares (0,5 puntos).
12. PAU25 Extraord Asturias 2025.2Pregunta 1. La tabla adjunta corresponde a la etiqueta de la información nutricional expuesta en la zona exterior del envase de un alimento ultra-procesado, los denominados palitos de cangrejo o surimi, un preparado disponible en tiendas de alimentación
.
Abreviaturas:
g: gramos
mg: miligramos (0.001 gramos)
μg: microgramos (0.000001 gramos)
Opción A
Indica qué diferencia las grasas saturadas, las monoinsaturadas y polinsaturadas. Indica cuál de los tres tipos tiene la temperatura de fusión más baja y explica por qué. (Calificación 1 punto)
Explica si el colesterol es o no un lípido anfipático e indica si tiene relación con alguna de las vitaminas que aparecen en la etiqueta de la información nutricional. Justifica tu respuesta. (Calificación 1 punto)
Explica cómo es posible que los lípidos se puedan transportar por la sangre de una zona a otra del organismo si son moléculas altamente hidrofóbicas y, por tanto, insolubles en un medio acuoso como la sangre. (Calificación 0.5 puntos)
Opción B
Indica qué compuestos de los que se enumeran en la etiqueta de la información nutricional presentan enlaces O-glucosílico y explica cómo se establece ese enlace. (Calificación 1 punto)
Indica cómo se establece un enlace N-glucosílico, pon un ejemplo de macromolécula con este tipo de enlace y explica si este enlace participa directamente en la formación de polímeros, esto es, en la unión repetitiva de pequeñas moléculas o monómeros para formar una macromolécula polimérica. (Calificación 1 punto)
Indica si con la información de la etiqueta nutricional se puede saber si el producto tiene un origen exclusivamente animal. Justifica tu respuesta. (Calificación 0.5 puntos)
13. PAU25 Extraord EXTREMADURA 2025.Pregunta 1.- Biomoléculas (2 puntos) y Metabolismo (0,5 puntos).
Opción A.
A1.- Identifique y nombre las siguientes biomoléculas a partir de las características que se indican (2 puntos:
0,5 puntos cada apartado):
a) Polihidroxialdehído. Forma parte de un dímero de origen vegetal con enlaces β(1-4) con función estructural. LA CELOBIOSA - DIMEROS DE GLUCOSA.
b) Liposoluble. Insaponificable. Origen animal. Regula la fluidez de las membranas biológicas.
c) Formado siempre por C, H, O y N, aunque pueden estar presentes otros biolementos. Desnaturalizable
mediante cambios de temperatura. Participa de manera directa en la contracción muscular.
d) Contiene C, H, O, N y P. Participa en la formación del ARN pero no en la del ADN.
A2.- La molécula descrita en el apartado a) se cataboliza en condiciones de anaerobiosis por las células
vegetales. (0,5 puntos):
a) Nombre de esta ruta y localización celular. (0,2 puntos). GLUCÓLISIS
b) Balance final de esta ruta metabólica (nombre y cantidad numérica de las moléculas que se producen). (0,3).
Opción B.
B1.- Identifique y nombre las siguientes biomoléculas a partir de las características que se indican (2 puntos:
0,5 puntos cada apartado):
a) Polihidroxicetona. Posee seis átomos de C. Isómero de la glucosa. Forma parte de la sacarosa. FRUCTOSA
b) Liposoluble. Insaponificable. Origen animal. Regula el desarrollo sexual y la función reproductora.
c) Polímero compuesto por A, G, C y U. Forma una doble hélice. Desnaturalizable mediante cambios de pH.
Aislado a partir de un virus.
d) Completamente hidrófobo. Su hidrólisis enzimática rinde alcohol y ácido graso. Reacción de saponificación
positiva.
B2.- La molécula descrita en el apartado a) forma parte de una ruta catabólica anaeróbica presente en todos
los seres vivos. Indique: (0,5 puntos)
a) Nombre de esta ruta y localización celular. (0,2 puntos).GLUCÓLISIS
b) Balance final de esta ruta metabólica (nombre y número de las moléculas que se producen). (0,3 puntos).
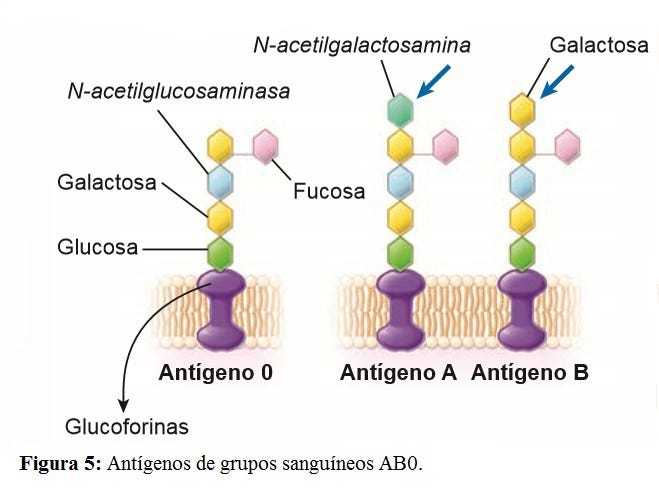
GLUCOCALIX. mensajes escritos en el idioma glucídico.
- Una persona del grupo A tendrá la enzima necesaria para añadir N-acetilgalactosamina como azúcar extra a la galactosa 5.
- Una persona del grupo B tendrá la enzima necesaria para añadir Galactosa como azúcar extra a la galactosa 5.
- Una persona del grupo AB tendrá ambas enzimas y sintetizan antígeno A y B.
- Una persona del grupo O carece ambas enzimas y sintetizan antígeno A y B.
Algún ejemplo de pregunta competencial.
Pared celular bacteriana - Peptidoglucanos o mureinas.
La penicilina es un antibiótico que inhibe la síntesis de los peptidoglucanos.
a) ¿Podría emplearse para tratar una enfermedad producida por virus? ¿Y por hongos (micosis)?
b) Explica de forma razonada por qué este antibiótico ataca a las bacterias y, sin embargo, no ataca a las células humanas.
PAU 25. CANTABRÍA. APARTADO 1 [1,25 puntos]. Bloque A. Las biomoléculas. Conteste a las preguntas de UNA SOLA de las siguientes opciones.
Opción 1 [1,25 puntos]. Para entretener a los bebés es habitual darles un trocito de pan seco para que lo mastiquen. Con el tiempo, la acción enzimática de la saliva lo vuelve dulce y les gusta. a) ¿Cómo se denomina la enzima responsable de este fenómeno y cuál es el enlace que rompe? b) ¿Sobre qué polímero está actuando y a qué familia de biomoléculas orgánicas pertenece dicho polímero? c) Indique otro polímero formado por las mismas subunidades, pero con una función estructural y no asimilable por los animales. d) Compare las estructuras de ambos polímeros y explique el motivo de las diferencias entre ellos.








































Comentarios
Publicar un comentario